国家食品药品监督管理局:肝功能异常患者和孕妇禁用龙必舒制剂
日前,国家药品监督管理局在网站上发布了关于修订龙双舒制剂说明书(以下简称"通知")的通知。根据药品不良反应评估结果,为进一步保障公众用药安全,国家药品监督管理局决定统一修改龙双舒制剂(包括胶囊、片剂)的说明书[不良反应](禁忌)和注意事项。
龙栓舒制剂规范修订要求显示,[不良反应]应包括显示以下不良反应的监测数据:恶心,呕吐,腹痛,腹胀,腹泻,胃部不适,口渴,肝脏生化指标异常,皮疹,瘙痒,头晕,头痛,心悸,乏力等。禁忌"项目应包括:孕妇禁忌,禁止对本品及其所含成分过敏,禁止肝功能异常。注意事项"应包括本产品的餐后推荐使用。应当按照药品说明书的功能处理和规定的使用剂量使用,不得超过药品的用量。服用本品如出现尿黄眼黄,皮肤黄染或肝脏生化指标异常,应立即停药,及时就医。长期用药应注意肝脏生化指标的监测。"

公告强调,所有上述药物的持牌人,应按照"药物注册及管理办法"等有关规定,根据有关指示的修订要求,修订有关指示,并於二0二一年一月二十五日前,报省药品监督管理部门备案。"修改内容涉及药品标签的,应当共同修改;说明书和其他内容应当与原批准的内容一致。自备案之日起生产的药品,不得继续使用原药品说明书。药品上市许可证持有人应当自申报之日起9个月内,更换已离开工厂的药品说明书和标签。
公告提醒药品上市许可证持有人应深入研究新的不良反应机制,采取有效措施,做好药品使用和安全宣传培训,引导医生和病人合理用药。临床医师应认真阅读上述药品说明书的修订内容,并根据新修订的用药说明书进行全面的效益/风险分析。用药前应仔细阅读药品说明书,使用处方药时应严格遵守医生的指示。
公告"要求省药品监督管理部门督促本行政区域内上述药品的药品许可证持有人,按照规定修改相应的说明书和更改标签、说明书,依法严厉查处违法行为。
 热点推荐
热点推荐-
 荟萃冰雪装备智者,共探产业创新路径 | 2025冬博会冰雪装备产业创新发展论坛圆满举办
荟萃冰雪装备智者,共探产业创新路径 | 2025冬博会冰雪装备产业创新发展论坛圆满举办 -
 “极光”闪耀,品牌领航 | 2025国际冬季运动领先品牌评选颁奖典礼盛大举行
“极光”闪耀,品牌领航 | 2025国际冬季运动领先品牌评选颁奖典礼盛大举行 -
 汇聚冰雪名城智慧,擘画冰雪经济蓝图 2025冬博会冰雪名城与冰雪新经济论坛成功举办
汇聚冰雪名城智慧,擘画冰雪经济蓝图 2025冬博会冰雪名城与冰雪新经济论坛成功举办 -
 中国冰雪文旅产业发展大会暨冬博会冰雪文旅创新融合发展论坛圆满举行
中国冰雪文旅产业发展大会暨冬博会冰雪文旅创新融合发展论坛圆满举行 -
 向世界 再出发 2025国际冬季运动博览会开幕
向世界 再出发 2025国际冬季运动博览会开幕 -
 投资中国基金启动 1160 亿元试运行 确权为赎回变现核心前提,夯实封转开业务根基
投资中国基金启动 1160 亿元试运行 确权为赎回变现核心前提,夯实封转开业务根基 -
 后冬奥时代,共探中小雪场新发展 2025国际冬季运动博览会雪场运营专场论坛成功举办
后冬奥时代,共探中小雪场新发展 2025国际冬季运动博览会雪场运营专场论坛成功举办 -
 山东省邹城市召开“提振文旅消费 丰富文化供给”新闻发布会
山东省邹城市召开“提振文旅消费 丰富文化供给”新闻发布会 -
 星际远航全球独创“歌全球AI音乐大会”创造世界奇迹,践行中国文化全球行先锋
星际远航全球独创“歌全球AI音乐大会”创造世界奇迹,践行中国文化全球行先锋 -
 Club Med地中海俱乐部2025年国庆假期业绩亮眼,持续显现强劲增长态势
Club Med地中海俱乐部2025年国庆假期业绩亮眼,持续显现强劲增长态势
 精选内容
精选内容-
 乐兔司获双料认证:连续两年销量第一,每批检测开创者铸就品质标杆
乐兔司获双料认证:连续两年销量第一,每批检测开创者铸就品质标杆 -
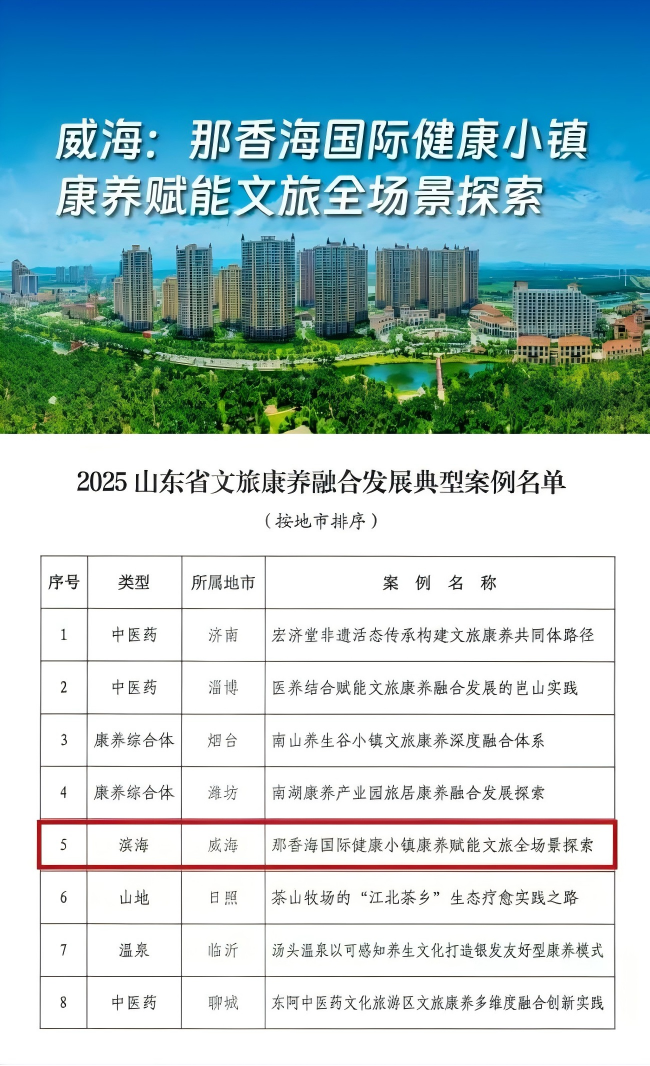 全省8席,威海唯一!那香海入选“山东省文旅康养融合发展典型案例”
全省8席,威海唯一!那香海入选“山东省文旅康养融合发展典型案例” -
 熊大爷社区运营秘籍:外卖万单店的私域流量密码
熊大爷社区运营秘籍:外卖万单店的私域流量密码 -
 全省8席,威海唯一!那香海入选“山东省文旅康养融合发展典型案例”
全省8席,威海唯一!那香海入选“山东省文旅康养融合发展典型案例” -
 全省8席,威海唯一!那香海入选“山东省文旅康养融合发展典型案例”
全省8席,威海唯一!那香海入选“山东省文旅康养融合发展典型案例” -
 熊大爷社区运营秘籍:外卖万单店的私域流量密码
熊大爷社区运营秘籍:外卖万单店的私域流量密码 -
 熊大爷社区运营秘籍:外卖万单店的私域流量密码
熊大爷社区运营秘籍:外卖万单店的私域流量密码 -
 从第一口到第N次:熊大爷如何用一只现包饺子攒下1.2亿“信任基金”
从第一口到第N次:熊大爷如何用一只现包饺子攒下1.2亿“信任基金” -
 从第一口到第N次:熊大爷如何用一只现包饺子攒下1.2亿“信任基金”
从第一口到第N次:熊大爷如何用一只现包饺子攒下1.2亿“信任基金” -
 从第一口到第N次:熊大爷如何用一只现包饺子攒下1.2亿“信任基金”
从第一口到第N次:熊大爷如何用一只现包饺子攒下1.2亿“信任基金”